Entre o prevenir e o remediar
É possível detectar mais FAs para prevenir os AVCs, ou podemos tratar melhor após o evento?
⌚ Monitoramento de FA com smartwatch. Ele quadruplica o diagnóstico, mas o que fazer depois?
🌊 Um oceano de possibilidades na prevenção secundária do AVC. Inibição do fator XI com asundexian reduz eventos, mas e o sangramento?
⚡ Quem choca mais? CDI subcutâneo ou transvenoso, qual tem mais choques inapropriados?
👀 Resposta do desafio de imagem na AngioTC da semana passada.
Estamos prontos para caçar o invisível?
por Diandro Mota
A fibrilação atrial (FA) é uma especialista em passar despercebida. Paroxística, frequentemente assintomática, muitas vezes só se revela quando já deixou sua assinatura mais temida: o AVC.
Por isso, a ideia de rastrear esses pacientes de forma contínua, não invasiva e escalável sempre foi atraente, mas faltava um modelo que realmente funcionasse na prática.
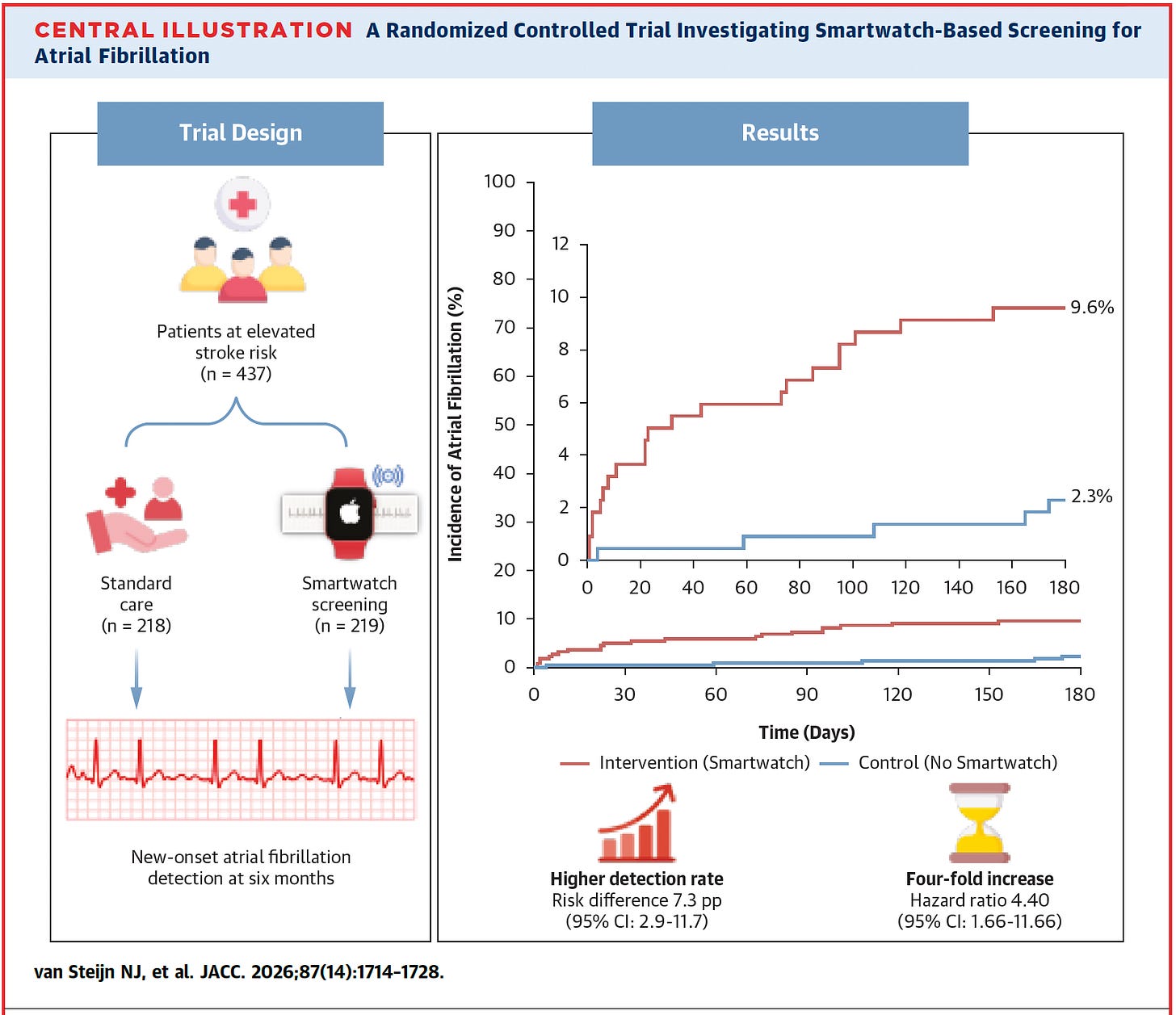
O estudo EQUAL, publicado no JACC 2026, traz exatamente essa provocação. Em um ensaio clínico randomizado com pacientes ≥65 anos e alto risco tromboembólico, a estratégia de monitoramento com smartwatch (Apple Watch) por seis meses foi comparada ao cuidado usual.
O grande diferencial do estudo foi a integração.
Detecção passiva por fotopletismografia → confirmação por ECG de uma derivação → envio automático dos traçados → revisão em até 24 horas por uma equipe especializada.
Diferente de outros estudos que focaram na avaliação da acurácia diagnóstica do wearable, esse associa o diagnóstico à avaliação clínica.
A detecção de FA foi de 9,6% no grupo smartwatch contra 2,3% no cuidado usual, com um aumento de cerca de quatro vezes na chance de diagnóstico.
Mais do que isso, o diagnóstico aconteceu mais cedo, um detalhe essencial em uma condição silenciosa e potencialmente devastadora.
Mais da metade dos casos detectados no grupo smartwatch era assintomática, enquanto no grupo controle todos os pacientes tinham sintomas. Ou seja, não estamos apenas antecipando diagnósticos, estamos acessando uma dimensão oculta da doença. E, como esperado, a maioria dos casos era paroxística, justamente o tipo de FA que escapa das estratégias tradicionais de monitoramento.
Claro, há um custo para essa sensibilidade. O valor preditivo positivo do algoritmo foi de cerca de 54%, o que significa que nem todo alerta é, de fato, fibrilação atrial.
E é aqui que o estudo acerta: nenhum diagnóstico foi feito sem validação humana. Cada traçado passou por revisão clínica antes de qualquer decisão terapêutica.
Todos os pacientes diagnosticados receberam anticoagulação conforme diretrizes, mostrando que o sistema não apenas detecta, mas conecta diagnóstico à ação.
Ainda assim, permanece a pergunta mais importante: detectar mais fibrilação atrial muda desfechos? Esse estudo não responde, e os próprios autores reconhecem que ainda precisamos de evidência para impacto em AVC, insuficiência cardíaca e mortalidade.
No fundo, o EQUAL não é um estudo sobre a eficácia dos relógios, que já conhecemos. É um estudo sobre modelo de cuidado, mostrando que é possível transformar o alerta digital em uma decisão clínica estruturada, segura e potencialmente escalável. E talvez o maior avanço seja justamente esse.
A pergunta não é se conseguimos detectar mais FA (isso já está claro), e sim se estamos prontos para lidar com o que vamos encontrar.
Um oceano de possibilidades
por Marcos Meniconi
Depois de um AVC, o maior medo do paciente não é o que já aconteceu, é o que pode acontecer de novo. E a cardiologia (e a neurologia) sabem bem disso.
Mesmo com antiagregantes, o risco residual segue alto. A pergunta que fica é: dá pra ir além sem pagar o preço do sangramento?
Foi exatamente nesse ponto que surge o OCEANIC-STROKE, um grande ensaio clínico publicado no NEJM que explorou uma nova via de anticoagulação: o fator XI.
A lógica é elegante. Diferente de outros fatores da coagulação, o fator XI parece ter um papel mais relevante na trombose patológica do que na hemostasia fisiológica. Em outras palavras: bloquear esse eixo poderia reduzir eventos isquêmicos… sem aumentar sangramento.
Vale lembrar o “pai” do OCEANIC-STROKE, o OCEANIC-AF (a grande decepção do congresso da ESC em 2024) foi interrompido precocemente ao demonstrar inferioridade do uso do Asundexian (um inibidor do fator XIa) quando comparado à apixabana na prevenção de AVC em pacientes com FA.
Dessa vez, os autores resolveram partir para uma população um pouco diferente.
Mais de 12 mil pacientes com AVC isquêmico não cardioembólico ou AIT de alto risco foram randomizados para receber asundexian (inibidor do fator XI) ou placebo, sempre em cima da terapia antiplaquetária padrão .
Resultados:
Menos AVC isquêmico: 6,2% no grupo asundexian vs. 8,4% no placebo (HR 0,74)
Menos eventos cardiovasculares maiores (morte CV, IAM ou AVC também reduzidos);
E o mais interessante: sem aumento de sangramento maior (1,9% vs. 1,7%)
Ou seja: reduziu eventos, sem pagar o preço clássico da anticoagulação .
Mas, talvez, o dado mais provocativo seja o conceito por trás. Historicamente, tentar combinar terapias antitrombóticas sempre esbarrou no mesmo problema: quanto mais potente, maior o risco de sangramento. Aqui, pela primeira vez em larga escala, vemos um sinal claro de dissociação entre trombose e hemostasia.
Trata-se de explorar uma via que pode redefinir a prevenção secundária do AVC, especialmente naquele paciente que já está “no limite” do tratamento convencional.
Claro, nem tudo são águas calmas. O benefício não foi uniforme em todos os cenários (por exemplo, sem redução significativa nos primeiros 90 dias), e ainda precisamos entender melhor onde essa estratégia se encaixa no mundo real: qual paciente ganha mais? Qual combinação faz mais sentido? E, principalmente, qual o impacto a longo prazo?
Quem choca mais?
por Maria Júlia Souto
Se você já implantou (ou indicou) um CDI, provavelmente já se fez essa pergunta: entre o subcutâneo e o transvenoso, qual “erra mais”? Ou melhor… qual choca mais quando não deveria?
Um patient-level meta-analysis reunindo os dois maiores estudos randomizados da área (PRAETORIAN e ATLAS), com mais de 1.300 pacientes e seguimento médio de 3,5 anos, trouxe a resposta mais robusta até agora.
De forma direta: os choques inapropriados são raros em ambos os dispositivos, mas ocorrem mais frequentemente com o CDI subcutâneo.
As taxas foram de 2,5 versus 1,5 eventos por 100 pacientes-ano (HR 1,61), um aumento relativo que chama atenção, mas com impacto absoluto relativamente pequeno.
Mas o dado que realmente importa não está na frequência, está no mecanismo.
Os choques inapropriados do S-CDI acontecem, em sua maioria, por oversensing: leitura inadequada de sinais cardíacos (onda T, onda P) ou interferência externa, como miopotenciais. Já no CDI transvenoso, o problema é outro: arritmias atriais, especialmente fibrilação atrial, que acabam sendo interpretadas como arritmias ventriculares e disparam terapias indevidas.
O editorial que acompanha o artigo ajuda a colocar esse cenário em perspectiva. Primeiro, reforça que esses achados já eram esperados, dado o sinal consistente observado nos estudos prévios. Segundo, e mais importante, destaca que as taxas globais são baixas, refletindo a evolução tecnológica dos dispositivos ao longo das últimas décadas. Não só isso: os mecanismos por trás dos choques inapropriados são, em grande parte, modificáveis.
E é aí que a decisão deixa de ser numérica e passa a ser estratégica.
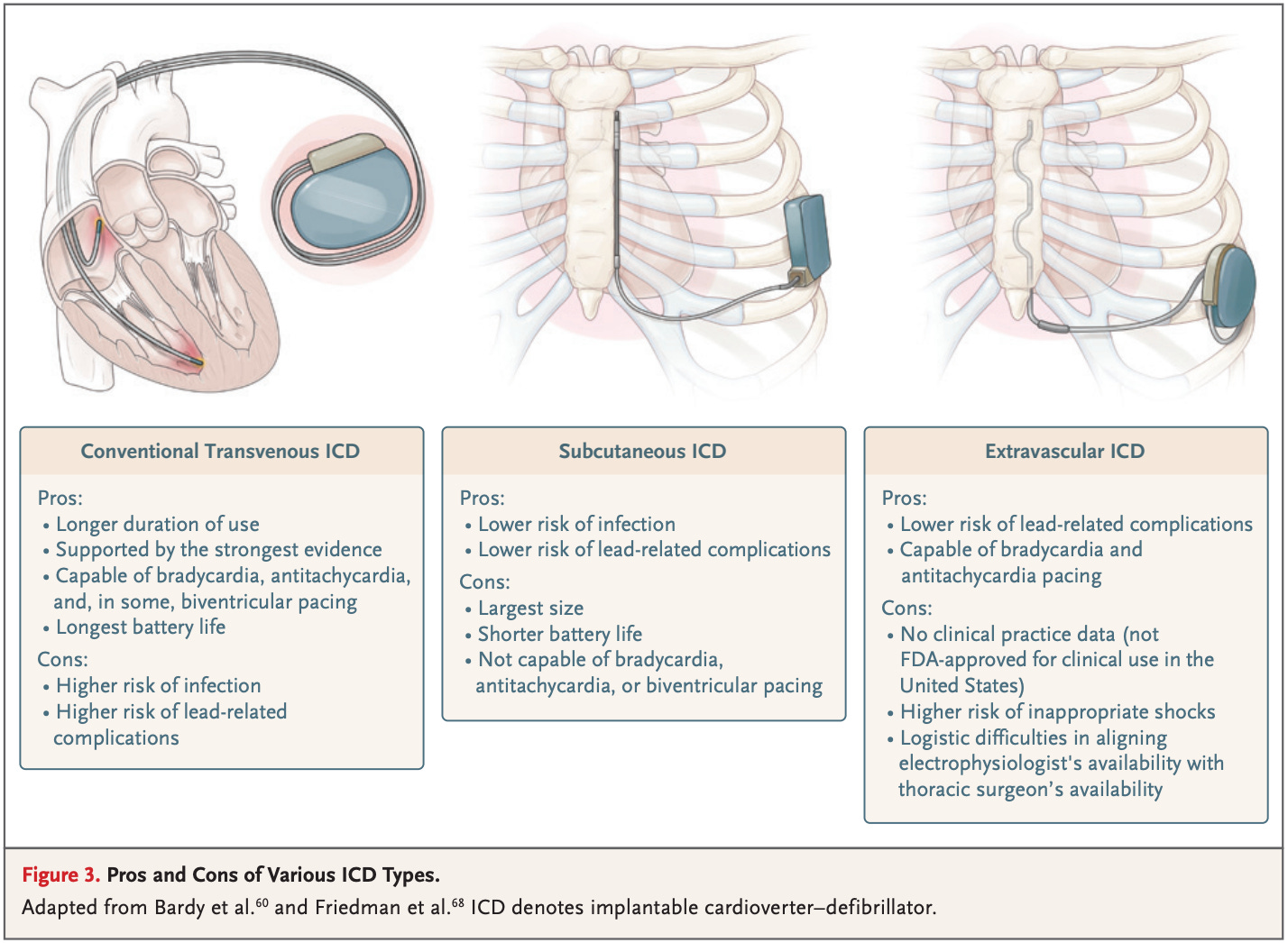
O S-CDI tende a ser mais atraente em pacientes jovens, sem necessidade de estimulação, nos quais evitar lead endovascular é uma prioridade. Já o CDI transvenoso mantém vantagem em cenários onde pacing é necessário, seja para bradicardia, terapia antitaquicardia ou ressincronização.
Trata-se de entender por que choca, e qual risco você está disposto a aceitar em troca do benefício estrutural.
A dica adicional de leitura fica por conta da revisão sobre os dispositivos implantáveis publicada no NEJM em 2024:
Resposta do desafio
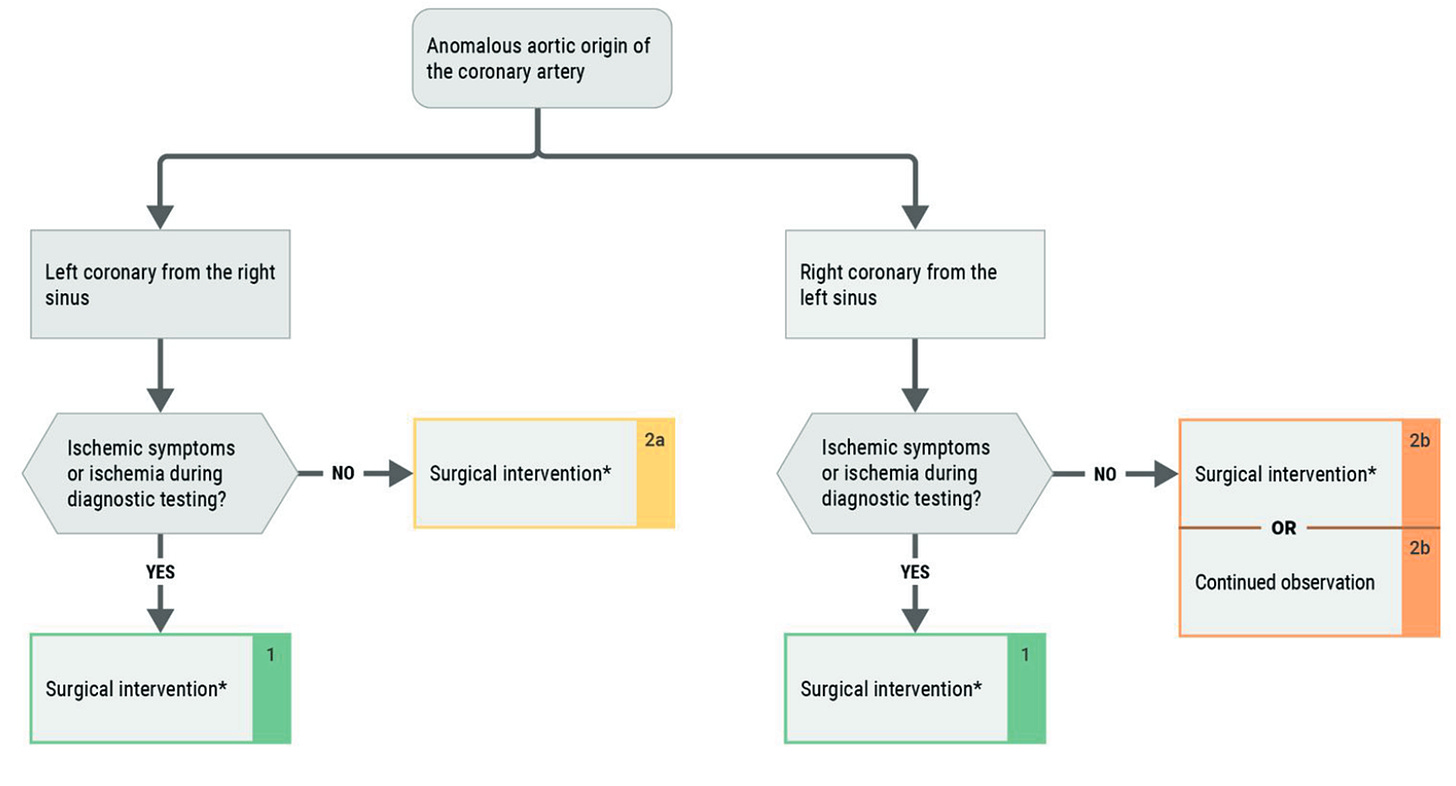
Na edição da semana passada, trouxemos um caso de origem anômala do TCE. A conduta nesses casos é essencialmente cirúrgica nesses casos, conforme proposto na última diretriz de cardiopatias congênitas do ACC/AHA.
Sem polêmica rs. A realização de prova funcional para avaliação de isquemia não estaria errada, podendo reforçar a indicação de abordagem na presença de teste positivo.
E, se você quiser ainda mais detalhes sobre o tema, vale a leitura da DozePrime sobre Origem Anômala de Coronárias:
Fique por dentro
🫀 Fibrose em tempo real: estamos começando a enxergar o coração “adoecendo”. Estudo publicado no JAMA com PET-RM usando inibidor da proteína de ativação de fibroblastos 46 marcado com gálio-68 ([68Ga]FAPI-46) mostra ativação persistente de fibroblastos na HFrEF, com padrões distintos entre etiologias e correlação com menor recuperação da função ventricular.
🥦 Comida como remédio: boa ideia, mas ainda sem impacto nos desfechos duros. Ensaio randomizado mostra que fornecer refeições ou alimentos frescos após internação por insuficiência cardíaca é viável e bem aceito, com melhora em qualidade de vida, mas sem redução de reinternações em 90 dias.
👦🏻 Kawasaki: corticoide ajuda no quadro agudo, mas não muda o que mais importa. Ensaio randomizado publicado no NEJM mostra que adicionar prednisolona reduz febre e necessidade de terapia de resgate, mas não diminui lesões coronarianas.
💉 Hormônios sexuais e trombose: risco que vai muito além dos anticoncepcionais. Revisão do NEJM mostra que diferentes terapias hormonais, da reposição à terapia de afirmação de gênero, impactam a coagulação e aumentam o risco trombótico conforme formulação e perfil do paciente.
👉🏼 Reforço positivo. Estudo observacional apresenta resultados satisfatórios da administração de inibidores de PCSK9 em pacientes com ateroesclerose sem eventos prévios. O uso da caneta conferiu menores eventos durante o período estudado.
🔄 Tireoide e coração: uma relação mais íntima do que parece. Revisão mostra que disfunções tireoidianas impactam múltiplos eixos cardiovasculares, de lipídios e pressão a arritmias e função ventricular.
⚡️ Ablação do nó AV na terapia de ressincronização: promessa que não se confirmou. No estudo CAAN-AF, pacientes com HFrEF e fibrilação atrial permanente não tiveram redução de mortalidade ou eventos de insuficiência cardíaca com ablação comparado ao controle de frequência medicamentoso.